Liquordrainage und thorakale Aortenchirurgie
Einführung
- Eingriffe an der thorakoabdominalen Aorta bergen das Risiko einer intra- bzw. verzögert postoperativ auftretenden Paraplegie
- Auch bei endovaskulärer Prothetik im thorakalen Bereich der Aorta descendens kann sie auftreten
- In der Literatur wird die Inzidenz bei offener Chirurgie mit 2.5 – 40%, bei endovaskulären Verfahren mit 0.5 – 10 % angegeben
- Die Ursache der Paraplegie ist eine spinale Ischämie durch verminderten distalen Aortendruck während dem intraoperativen aortalen Crossclamping und/oder die nachfolgende Reperfusion mit konsekutivem Rückenmarksödem
- Ziel einer Liquordrainage ist somit die Vermeidung von Rückenmarksischämien durch Optimierung der Rückenmarksperfusion
- Aber auch eine anatomische oder thrombotische Unterbrechung von zuführenden Segmentarterien sind weitere mögliche Ursachen
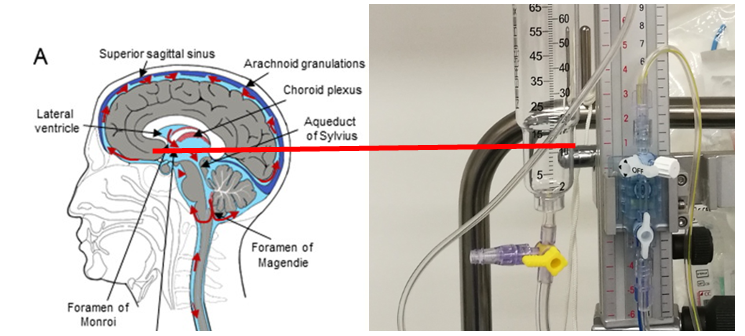
- Die Durchblutung des Rückenmarks erfolgt über die longitudinal zum Rückenmark verlaufende Arteria spinalis anterior und zwei posterolateral gelegene Spinalarterien
- Diese Gefässe entspringen aus den Vertebralarterien und werden segmental aus der Aorta thoracalis und lumbalis gespeist
- Die grösste dieser segmentalen zuführenden Arterien ist die Arteria Adamkiewicz, die der unteren Aorta thoracalis entspringt
- Das Risiko eines Schadens ist abhängig von der Lage und Ausdehnung des Aortenaneurysmas
- Hinzu kommt der Grad der Kollateralperfusion über je nach Lokalisation A.vertebralis, Viszeralgefässe oder die A. illiaca interna
Aorteneingriffe mit besonders hohem Paraplegierisiko
- Notfallmässige Eingriffe
- Lange Crossclamping-Zeiten
- Postoperative Hypotonie
- Hohes Alter
- Schwere Arteriosklerose
- Status nach Aortenchirurgie
- Diabetes mellitus
- Überstenting der A. subclavia links oder A. iliaca interna
- Stentlänge >20cm
Grundsätze
Grundsatz 1
- Cerebrospinaler Perfusionsdruck (SCPP) = MAP – CSF Druck, beziehungsweise MAP – RAP
- Der höhere von beiden (CSF oder RAP) ist entscheidend
- Entsprechend erwarten wir, durch eine Erhöhung des MAP und/oder eine Senkung des Liquordrucks durch eine lumbale Liquordrainage eine Erhöhung des Rückenmarksperfusionsdrucks
- Evidenz vorhanden für Inzidenzreduktion von postoperativer Paraplegie bei perioperativer Anwendung einer lumbalen Liquordrainage in Kombination mit Anhebung bzw. Korrektur des MAP
- Die Liquordrainage wurde auch bei einer erst postoperativ aufgetretenen Paraplegie mit Erfolg eingelegt
Grundsatz 2
- MAP soll in einem hohen Bereich gehalten werden, in Zahlen 80 – 100 mmHg
- Dieser Wert soll allenfalls auch in der postoperativen Phase für 24 – 48 h aufrechterhalten werden
- Beim Auftreten von neurologischen Ausfällen allenfalls höher und auch länger
Grundsatz 3
- Da das Anheben des Perfusionsdruckes nicht immer genügend ist, muss in ausgewählten Fällen präoperativ oder bei neurologischen Ausfällen auch postoperativ eine Liquordrainage gelegt werden
Liquordrainage
- Die Liquordrainage ist eine der häufigsten Interventionen zur Vermeidung von Rückenmarksischämien
- In der Literatur werden verschiedene Zielwerte für die Liquordrainage angegeben
Die meisten bewegen sich im Bereich von 10 bis 15 mmHg. Bei neurologischen Symptomen kann allenfalls bis auf 5 mmHg gesenkt werden
Die maximal pro Stunde erlaubte Drainage von Liquor beträgt rund 20 ml
- Bei offener Chirurgie kann nach Cross Clamping der Liquordruck abrupt ansteigen
- Dies wegen einer durch den gesteigerten Sympathikotonus bedingten Vasokonstriktion
- Als Folge davon wird der venöse Abfluss behindert und der CSF Druck steigt an
Komplikationen der Liquordrainage
- Bruch des Katheters
- Infektion
- Liquorleck
- Neuroaxiales Hämatom (subdural oder epidural)
- Intrakranielles Hämatom wegen Druckschwankungen durch Ablassen von Liquor (Kopfschmerzen, Abducensparese oder Subduralhämatome durch Zerreissen von Brückenvenen)
- Postdural puncture headache (~ 10%, 1/3 braucht Blood Patch)
Indikationsstellung
- Mit dem Gefässchirurgen zusammen unter Beachtung der Kontraindikationen Formen
| Präoperativ | Postoperativ |
|---|---|
| Elektive Einlage | Notfallmässig bei neu aufgetretenen Lähmungen |
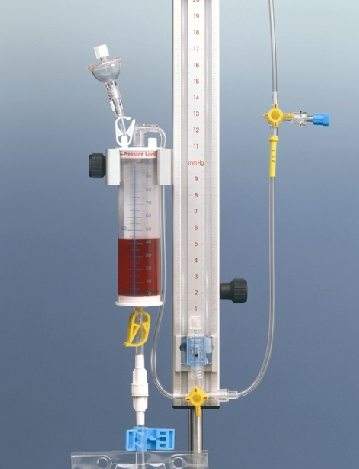
Material Liquordrainagekatheter
- Katheter und das Drainagesystem befindet sich hinter dem Saal 5 bei der OP Technik im Schrank (Anästhesie ist ageschrieben)
- Das spezielle Transducerkabel muss vom ZIM am inkl. der Messlehre geholt werden (Wenn alle in Gebrauch 6 Ost anfragen)
Einlage der Liquordrainage
- Gerinnung: Gleich wie bei PDK-Einlage
- Sterilität: Einlage mit Mantel
- Technik:Punktion: L4/L5 mittels Loss of resistance
- Vorschieben des Katheters in Liquorraum 8 – 10 cm über Punktionstiefe (mindestens)
- PDK Set Vorbereitung ggf zu zweit (einer bereitet den Katheter vor: Baden in NaCl 0.9%, Vorfüllen der Halterung des Drahtes, Einfädeln des Drahtes und Führung des Katheters)
- Nullpunkt auf Höhe des rechten Vorhofes (= phlebostatische Achse) oder äusserer Gehörgang, beide Methoden werden in der Literatur beschrieben. Dies entspricht ungefähr dem nicht direkt bestimmbaren Foramen Monroi
Cave: Nicht an Transducersystem mit Druckspülung anhängen; primär Drainageset geschlossen haltenLiquoraspiration immer mit neuer Spritze (da sonst Gefahr Spritzenstempel unsteril zu machen)
- Einlage der Liquordrainage einen Tag präoperativ durch die Anästhesie
- Überwachung auf ZIM / AWR bis zum OP-Termin am Folgetag
- Einlage entspricht dem Vorgang einer Lumbalpunktion, Katheter wird über eine Tuohy Kanüle in den Spinalraum gelegt (4.5F)
- Der Druck wird auf dem Philips Monitor als ICP benannt
- «Genullt» wird sobald der Transducer mittels Laserpointer auf die richtige Höhe (Höhe Foramen Monroi) gebracht wurde
- Durch Verschieben des Reservoirs am Messsystem wird der gewünschte Liquordruck eingestellt (hier 10mmHg)
- Dadurch wird über die Höhendifferenz Liquor drainiert bis zum eingestellten Liquordruck Es dürfen maximal 20 ml/h abgelassen werden
- Merke: Rote Skalierung = mmHg, Blaue Skalierung = cmH2O
- Bei Verdacht auf eine Occlusion des Systems kann versucht werden dieses mit einer 2 ml Spritze NaCl 0.9%, das System zu entstopfen
Liegedauer der Drainage
- Entfernung der Drainage so rasch wie möglich. Meistens ist dies 24- 48 h Sunden nach dem Eingriff – falls keine neurologischen Probleme – möglich
- Gerinnung beachten (Vorschlag: INR < 1.3, Tc > 50`000 / µl, Heparin 4 Stunden vorher stoppen)
- LWMH mindestens 12 h vorher stoppen
- Heparin wieder starten: 2- 4 h nach Ziehen
Differentialdiagnose einer Liquordruckerhöhung
- Ein Anstieg des Liquordruckes kann auch folgende Ursachen haben
- Diese Parameter sollen unbedingt parallel zum SCPP-Management beachtet werden
| Anstieg des ZVDs (venöse Stase) | Azidose | Hohes CO2 (Vasodilatation) |
|---|
Literatur
- John G.T. Augoustides; Marc E. Stone; Benjamin Drenger; Novel approaches to spinal cord protection during thoracoabdominal aortic intervention. Current Opinion in Anaesthesiology. 27(1):98–105, FEB 2014
- Christine A. Fedorow; Michael C. Moon; W. Alan Mutch; Hilary P. Grocott; Lumbar Cerebrospinal Fluid Drainage for Thoracoabdominal Aortic Surgery: Rationale and Practical Considerations for Management. Anesthesia & Analgesia. 111(1):46–58, JUL 2010
- Spinal Cord Protection with a Cerebrospinal Fluid Drain in a Patient Undergoing Thoracic Endovascular Aortic Repair (Lam CH, J Vasc Interv Radiol 2010)
- Cerebrospinal Fluid Drainage During TEVAR (Mehta M, Endovascular Today, 2008)
- Protocol implementation of selective postoperative lumbar spinal drainage after thoracic aortic endograft (Keith CJ, Journal of Vascular Surgery, 2012)
- Standard of Practice for the Endovascular Treatment of Thoracic Aortic Aneurysms and Type B Dissections (Fanelli F, Cardiovasc Intervent Radiol, 2009)
- The use of lumbar drains in preventing spinal cord injury following thoracoabdominal aortic aneurysm repair: an updated systematic review and meta-analysis (Khan NR, J Neurosurg Spine,2016)
Mitwirkende Autor/innen